
背景
研究表明,2′-岩藻糖基乳糖(2′-FL)能特异性刺激双歧杆菌属的增殖,建立健康的肠道微生物环境。大肠杆菌O157是一种常见的病原菌,可导致严重的出血性结肠炎和溶血性尿毒综合征(HUS),特别是对儿童、老年人和免疫力低下者。由于其毒性强且耐药性高,找到有效的预防和治疗方法非常重要。在此背景下,2′-FL作为一种功能性食品成分,可能在预防和缓解大肠杆菌O157感染中发挥重要作用。
PART.1
研究设计和方法
本研究采用小鼠感染模型,通过饲喂2′-FL后,分析其对肠道感染大肠杆菌O157的抑制效果。实验包括提取小鼠盲肠内容物中的细菌DNA,进行PCR扩增和基因分析,并使用16S rDNA基因测序来分析肠道微生物组。炎症水平通过测量血液、回肠和结肠中的IL-6、TNF-α和IL-1β含量来评估。此外,使用qPCR方法检测黏蛋白-2(MUC2)和紧密连接蛋白相关基因的表达水平。
PART.2
主要发现
1. 2′-FL抑制大肠杆菌O157在肠道中的定植
在回肠和结肠中,2′-FL组的大肠杆菌O157定植率显著低于对照组(MC组),分别为8.63% ± 6.87%和6.16% ± 2.25%。这表明2′-FL具有显著的抗病原菌定植效果,有助于减少肠道中的病原菌负担。
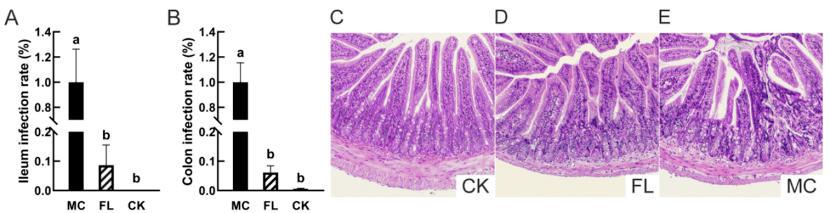
图1:大肠杆菌O157在回肠中的定植和回肠病理切片。(A)回肠中的定植;(B)结肠中的定植;(C)空白组(CK)的回肠组织切片代表图像(HE染色,100×);(D)FL组(HE染色,100×)的回肠组织切片代表图像;(E)模型对照组(MCG)的回肠组织切片代表图像(HE染色,100×)
2. 对肠道微生物组成和群落结构的影响
在门水平上,长时间补充2′-FL显著减少了厚壁菌门(Firmicutes)和帕特斯菌门(Patescibacteria)的生物数量,而拟杆菌门(Bacteroidetes)和变形菌门(Proteobacteria)的生物数量有所增加。具体来说,在属水平上, Parabacteroides, Eubacterium, Mucispirillum, Anaerotruncus和Alistipes显著减少,这些变化反映了2′-FL对肠道微生物生态平衡的显著影响。此外,2′-FL组表现出更高的多样性和稳定性。这种变化不仅有助于抵御病原菌的定植,还可能通过促进有益菌的生长来改善宿主的整体健康状况。
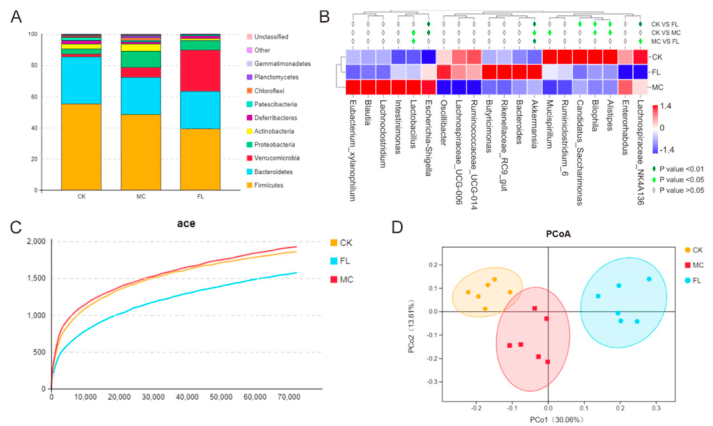
图2:不同组小鼠肠道微生物组的相对丰度、多样性和功能预测:(A)门;(B)属;(C)稀释曲线;
(D)基于操作分类单元(OTU)结果的PCoA分析
3.炎症水平和基因表达以及宿主免疫反应的影响
2′-FL显著降低了小鼠回肠和结肠中的炎症细胞因子(IL-6, TNF-α和IL-1β)水平,这表明2′-FL能够有效抑制由病原菌感染引起的肠道炎症反应。同时,2′-FL上调了结肠中黏蛋白-2(MUC2)和紧密连接蛋白基因的表达,这些基因的表达增加有助于增强肠道屏障功能,减少病原菌的侵入和定植。此外,补充2′-FL后,宿主免疫系统表现出更好的调节能力,具体表现为促炎和抗炎细胞因子的平衡。这种免疫调节作用可能是2′-FL通过肠道微生物群介导的一种间接效应。
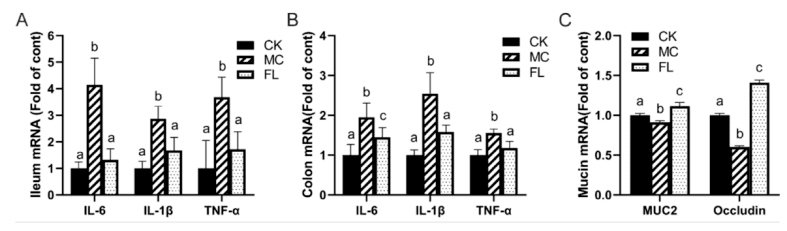
图3:炎性细胞因子和粘蛋白的相对 mRNA 水平,均与β-肌动蛋白 mRNA 表达正常化(A)回肠中的炎性细胞因子;(B)结肠中的炎性细胞因子;(C)结肠中粘蛋白的表达。不同字母(a-c)表示各组间同一因子差异显著(p<0.05)。
讨论和展望
研究表明,2′-FL在调节肠道微生物群和降低病原菌定植方面具有显著效果,特别是对大肠杆菌O157有抑制作用。此外,2′-FL对肠道炎症和屏障功能的改善也得到了验证。然而,进一步的研究仍需探讨其具体的机制和在其他病原菌感染中的应用潜力。未来研究可以通过探索2′-FL与其他益生元和益生菌的协同作用,来揭示其在肠道健康中的全面作用。
参考文献
[1] Wang Y , Zou Y , Wang J ,et al.The Protective Effects of 2′-Fucosyllactose against E. Coli O157 Infection Are Mediated by the Regulation of Gut Microbiotathe Inhibition of Pathogen Adhesion[J].Nutrients, 2020, 12(5):1284.DOI:10.3390/nu12051284.
