
背景
坏死性小肠结肠炎(NEC)是早产儿最常见的致死性肠道疾病,以肠缺血、坏死和全身性炎症为特征,死亡率高达40%。尽管母乳喂养被证实可显著降低NEC风险,但其机制尚未完全阐明。研究发现,母乳低聚糖(HMO),尤其是2′-岩藻糖基乳糖(2′-FL)具有免疫调节、维护肠道健康等重要作用。已有证据表明,当肠道炎症反应过度激活时,会抑制血管舒张关键酶eNOS的表达,导致肠道微循环障碍,从而加剧NEC的病理进程。基于此,本研究提出2′-FL可能通过上调eNOS表达并改善肠道血流灌注,最终缓解NEC的发展。
PART.1
研究设计和方法
研究采用新生小鼠NEC模型,通过配方奶喂养联合缺氧刺激模拟早产儿肠道损伤。实验分为四组:母乳喂养组、配方奶喂养组(NEC组)、配方奶+2′-FL干预组及eNOS基因敲除(eNOS⁻/⁻)组。通过进行组织病理学评分、肠道灌注成像、qRT-PCR检测炎症因子及eNOS表达,来评估2′-FL的保护作用。此外,通过16S rRNA测序分析肠道菌群变化;HUVEC实验进一步验证2′-FL对eNOS的直接调控作用,并以L-NIO/DPI药理学抑制剂阻断eNOS活性作为阴性对照。
PART.2
主要发现
1.2′-FL显著减轻NEC病理损伤
在新生小鼠坏死性小肠结肠炎(NEC)模型中,配方奶中添加2′-FL使NEC严重程度评分显著降低,肠黏膜结构完整性接近母乳喂养组水平。同时,促炎因子IL-6、IL-1β的表达降至原水平的一半以上,表明2′-FL能有效抑制肠道炎症反应并维持组织稳态。
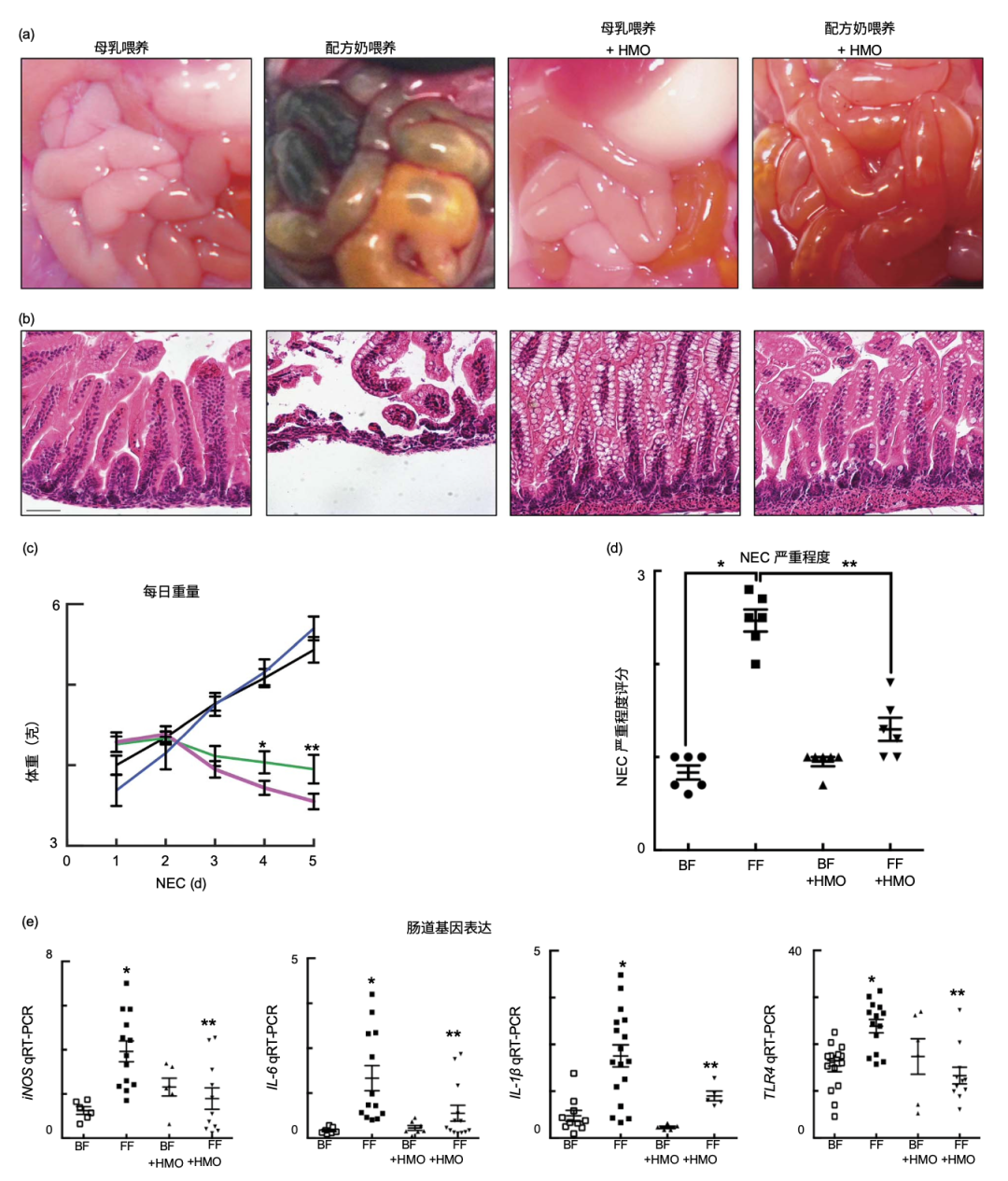
图1:在婴儿配方奶粉中加入2’-FL,可减轻新生小鼠坏死性小肠结肠炎(NEC)的严重程度
2.2′-FL通过上调eNOS表达改善肠道流血
研究证实,2′-FL通过上调内皮型一氧化氮合酶(eNOS)的表达,显著恢复肠道微循环灌注,使肠道绒毛灌注指数大幅提升,与母乳喂养组相当。证据显示,在eNOS基因敲除(eNOS⁻/⁻)小鼠或使用eNOS抑制剂后,2′-FL的保护作用完全消失,明确其机制依赖于eNOS介导的血管舒张功能。
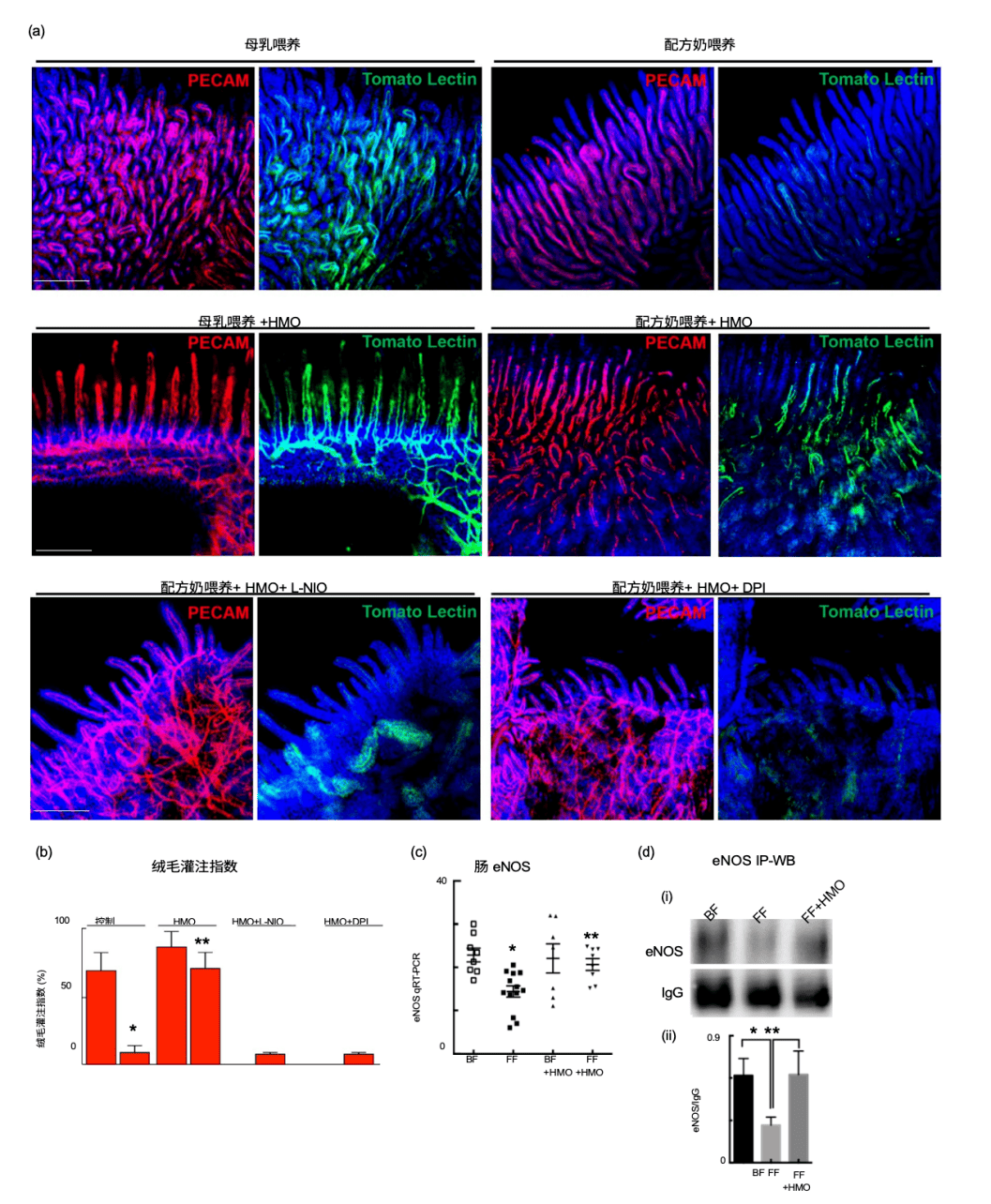
图2:通过上调eNOS的表达,补充2’-FL的配方奶能增强坏死性小肠结肠炎(NEC)的肠系膜灌注
3.2′-FL直接调控信号通路上调eNOS表达
体外实验(HUVEC细胞)进一步验证,2′-FL可逆转脂多糖LPS诱导的eNOS表达抑制,并直接促进eNOS mRNA的合成。该发现为体内研究提供了分子层面的机制支持,表明2′-FL能够从根源上改善肠道供血,从而对抗NEC。
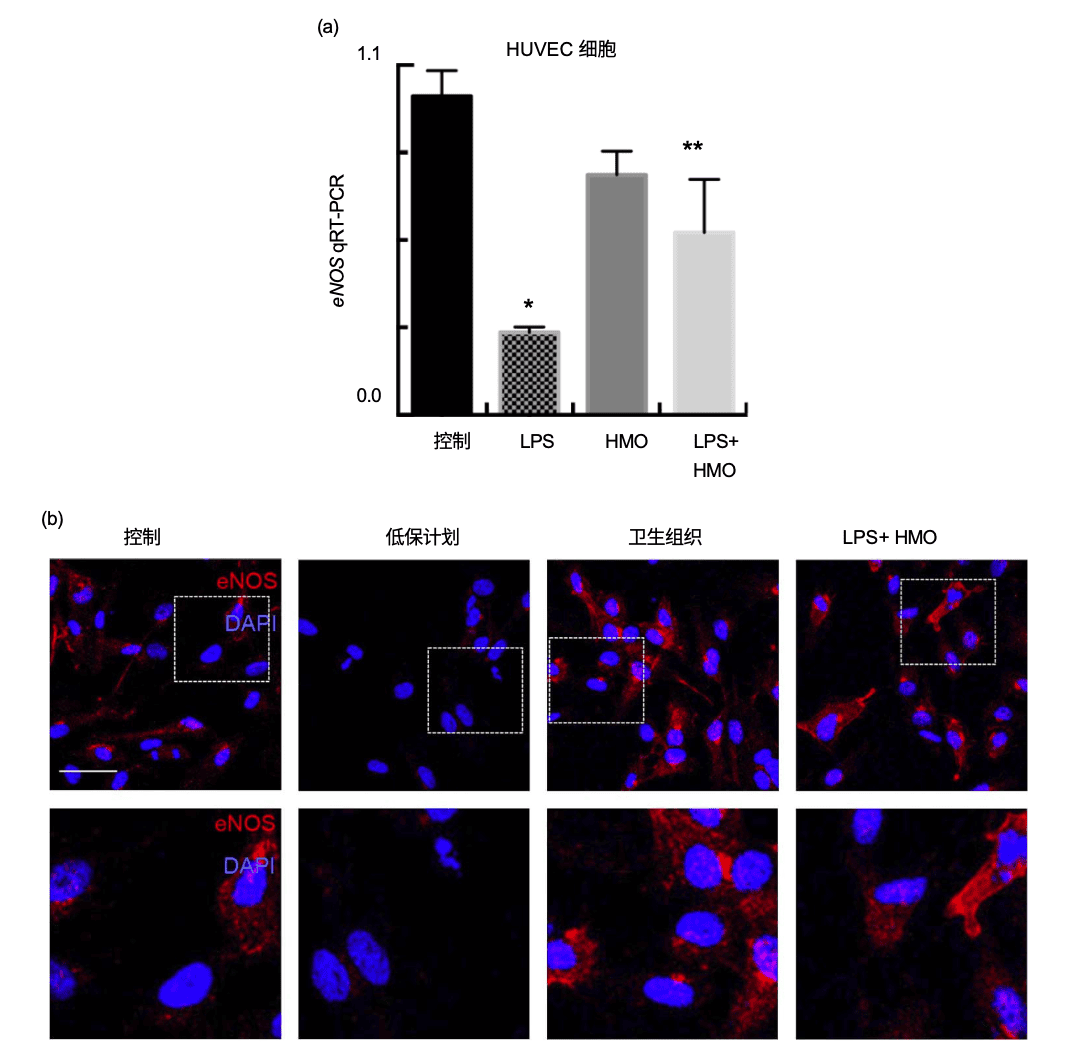
图3:2’-FL在HUVEC中增强了eNOS的表达
4.2′-FL对肠道菌群的影响为次要效应
尽管2′-FL干预后肠道菌群中瘤胃菌科(Ruminococcaceae)丰度增加,但β多样性分析表明菌群变化与NEC严重程度无直接关联。这一结果显示,2′-FL的核心保护作用主要源于其对肠系膜血流的调控,而非微生物组调节。
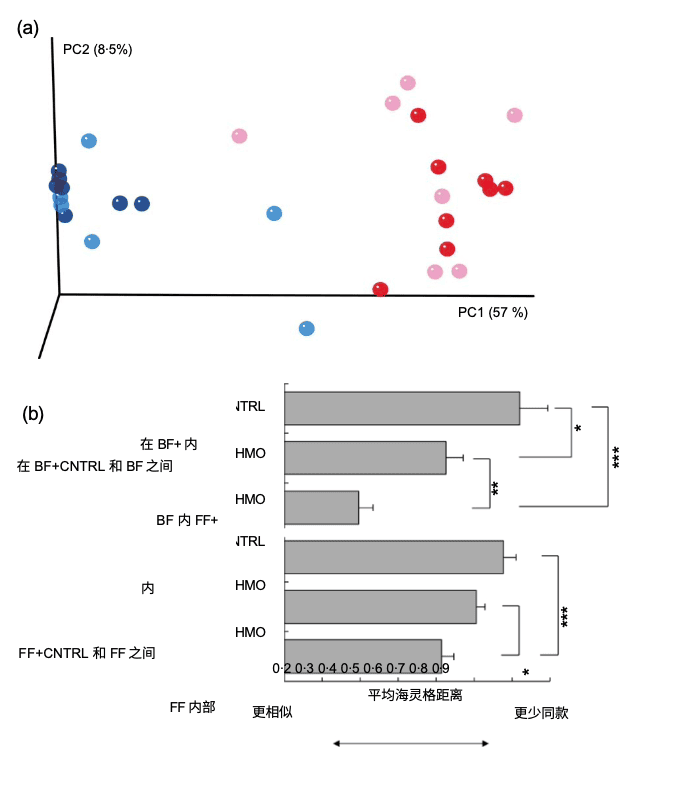
图4:用2’-FL处理的小鼠微生物区系的β多样性分析
讨论和展望
本研究揭示了2′-FL能够通过上调血管舒张关键酶eNOS的表达,改善肠道血流,从而有效缓解坏死性小肠结肠炎(NEC)。这一发现不仅拓展了HMO的应用范围,也为早产儿配方奶的优化提供了潜在方向。未来的研究可进一步探索2′-FL在临床中的应用价值,随着对HMO作用机制的深入探索,或能开发出更有效的NEC预防方案,为早产儿健康带来新的希望。
参考文献
[1] Good, Misty, et al. "The Human Milk Oligosaccharide 2′-Fucosyllactose Attenuates the Severity of Experimental Necrotising Enterocolitis by Enhancing Mesenteric Perfusion in the Neonatal Intestine." British Journal of Nutrition, vol. 116, no. 7, 2016, pp. 1175-1187, doi:10.1017/S0007114516002944.
