
背景
肠道屏障是维持肠道健康和免疫稳态的重要防线,其功能障碍与多种慢性疾病密切相关。母乳中的母乳低聚糖(HMO),尤其是2′-岩藻糖基乳糖(2′-FL),在调节菌群、抗炎免疫及维持肠道屏障完整性方面展现出广泛的生物学活性。已有研究显示,HMO不仅可作为益生菌生长的“碳源”,其代谢产物亦可能通过特定机制增强上皮屏障功能。本研究聚焦于2′-FL(本研究中2′-FL样品由虹摹生物科技有限公司生产)如何通过调控双歧杆菌DNG6的表面蛋白,缓解脂多糖(LPS)诱导的体外肠屏障损伤,深入揭示其作用机制。
PART.1
研究设计和方法
本研究以Caco-2肠上皮细胞单层构建体外屏障模型,模拟LPS诱导的肠道炎症。将双歧杆菌DNG6分别在乳糖(Lac)、半乳糖寡糖(GOS)和2′-岩藻糖基乳糖(2′-FL)为唯一碳源的条件下培养,提取其表面蛋白(分别标记为Sp-L、Sp-G、Sp-F),并干预LPS处理的Caco-2细胞,检测细胞活力、细胞毒性、炎症因子表达及紧密连接蛋白水平。
PART.2
主要发现
1. 2′-FL提升细胞活力,降低细胞毒性
研究显示,LPS处理显著降低Caco-2细胞活力,Sp-F(2′-FL处理组)在800–1000 μg/mL浓度下可将细胞存活率提升至88%以上,显著优于Sp-L和Sp-G。同时,Sp-F(2′-FL处理组)显著降低了反映细胞膜完整性的乳酸脱氢酶(LDH)释放水平,表明其在缓解细胞膜损伤方面效果显著。
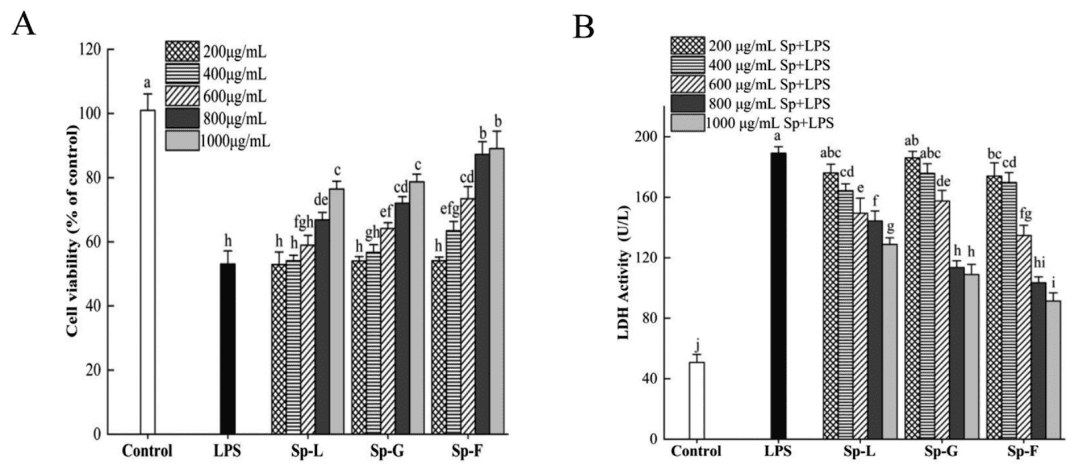
图1:表面蛋白对 LPS 诱导的 Caco-2 细胞活力和 LDH 活性的影响
2. 2′-FL抑制炎症反应,增强免疫调节
LPS显著诱导促炎因子TNF-α、IL-6和IL-1β表达,而Sp-F(2′-FL处理组)显著抑制分泌水平,分别降低53.46%、35.91%和37.05%;同时,抗炎因子IL-10水平提升至LPS组的140.13%,表明其具有良好的免疫调节功能。
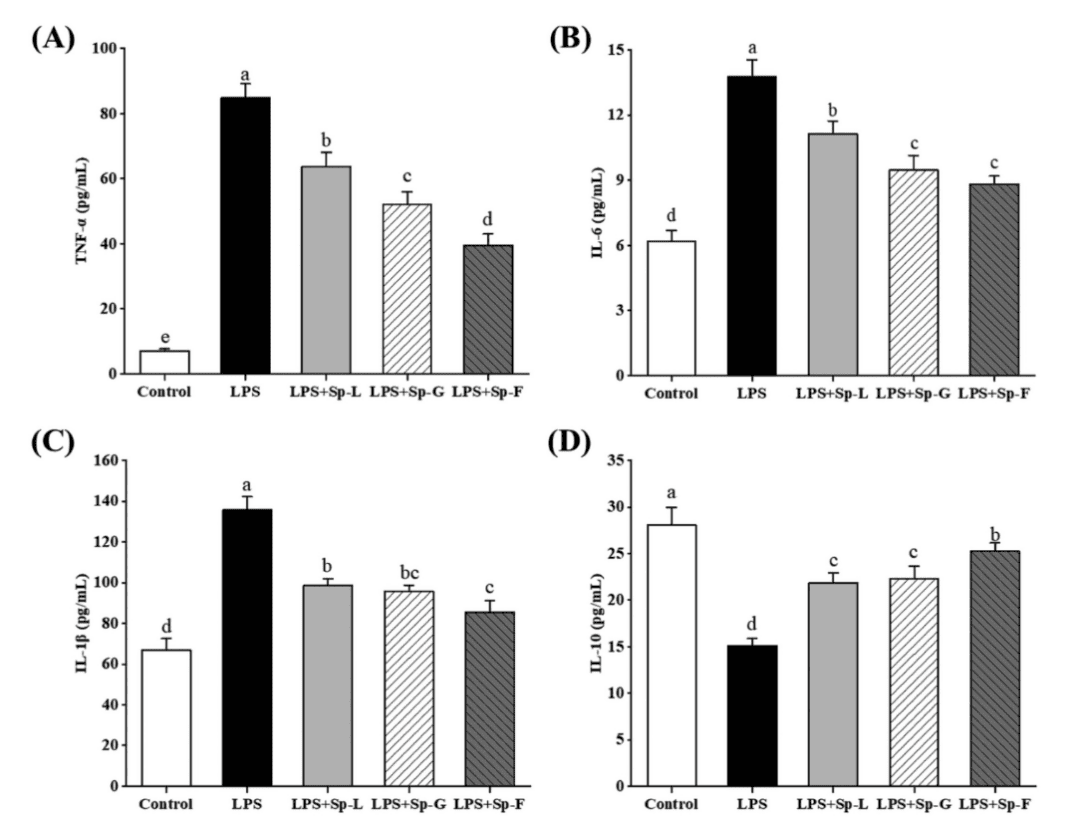
图2:表面蛋白对 LPS 诱导的 Caco-2 细胞单层屏障中 TNF-α、IL-6、IL-1β 和 IL-10 表达的影响
3. 2′-FL修复屏障结构,增强细胞连接
体外实验在LPS抑制紧密连接蛋白ZO-1、Claudin-1、Occludin表达的基础上,Sp-F(2′-FL处理组)显著提升三者mRNA表达(分别增加146.21%、268.53%、137.22%)及蛋白表达水平。ZO-1、Claudin-1、Occludin为上皮细胞间的主要紧密连接蛋白,是维持肠道屏障完整性、防止有害物质渗透的重要结构。结果显示,Sp-F(2′-FL处理组)能修复肠上皮屏障,改善细胞间连接完整性。
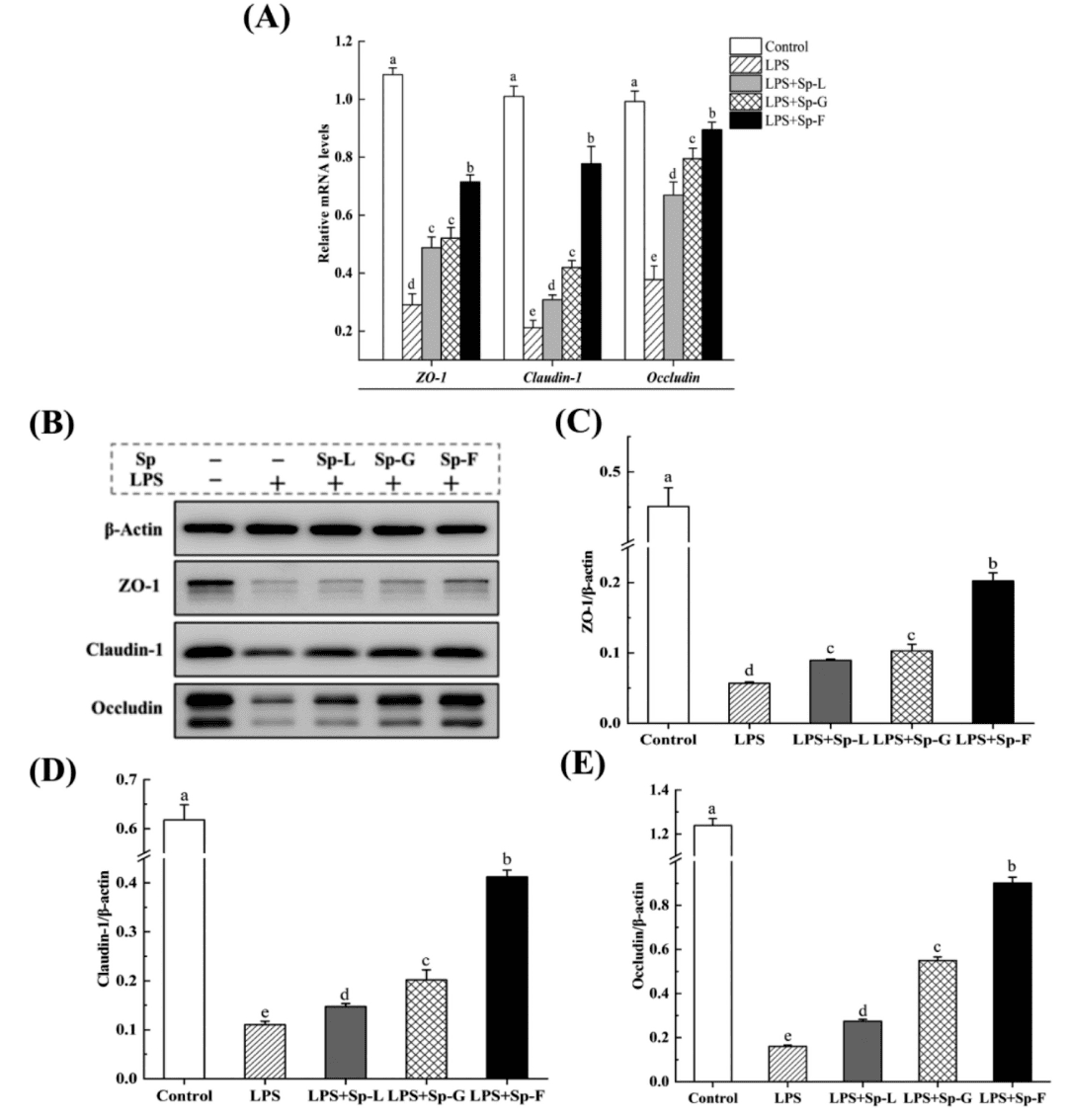
图3:表面蛋白对蛋白mRNA和蛋白表达的影响
讨论和展望
本研究从“菌体表面蛋白”角度揭示了2′-FL(本研究中2′-FL样品由虹摹生物科技有限公司生产)在维持肠道屏障稳态方面的机制:通过促进双歧杆菌DNG6表面蛋白表达,显著缓解LPS诱导的炎症损伤,增强肠道紧密连接蛋白表达。这一发现不仅扩展了HMO作用的分子机制认知,也为婴幼儿配方食品中HMO的功能应用提供了理论支持。未来可进一步结合动物模型和临床研究,探索其在早产儿、炎症性肠病等人群中的应用潜力。
参考文献
[1] Zhao, J., et al. "Surface Proteins of Bifidobacterium Bifidum DNG6 Growing in 2′-FL Alleviating LPS-Induced Intestinal Barrier Injury in vitro." Journal of Dairy Science (2024): S0022-0302.
